ヘモビジランス
ヘモビジランスとは
ヘモビジランス(Haemovigilance:血液安全監視)とは、血液製剤について、献血の段階から輸血患者の追跡調査までの全過程に関連するすべての有害事象を監視し、その原因を分析評価することにより適切な対応策を示し、被害の拡大を防ぐことです。
世界のヘモビジランス
欧州では、いわゆる「血液法」に相当する法律の有無や運用が国ごとに異なります。EU加盟国においては、欧州指令(EU Directive)により、ヒト血液の安全性及び品質にかかる基準(2002/98/EC)、技術的要件(2004/33/EC)、トレーサビリティと有害事象報告(2005/61/EC)、品質システム(2005/62/EC)、等が定められており、加盟国はこれらに従うと共に、各国それぞれのヘモビジランスシステムを運用しています。血液事業者の形態や、有害事象等を取り扱う組織・部門は国によりさまざまであり、国が直接関与する場合、赤十字が関与する場合、独立の血液事業者がある場合等、各国の事情に合わせて構成されています。有害事象の報告規定も、フランスのように全ての有害事象報告が義務化されているもの、イギリスのSHOTのように重篤な有害事象のみ自発的に報告するもの等、その形態はさまざまです。有害事象には輸血副作用だけではなく、採血副作用も含まれます。
米国では、2006年に、米国保健福祉省(HHS)と民間血液事業者によりUS Biovigilance Networkが結成されました。ここではヘモビジランスモジュールとして、輸血副作用の種類ごとに定義や判断基準などを示し、副作用症例ごとにオンラインで報告できるシステムが構築されています。採血時の副作用についても同様に報告できるようになっています。
発展途上国においては、WHOのBlood Transfusion Safety Programの一環として、各国の実情に合わせた形でのヘモビジランスシステムの構築が進められています。
日本のヘモビジランス
日本赤十字社は日本で唯一の採血事業者であり、輸血用血液製剤の製造販売業者です。日本では輸血用血液製剤は医薬品に該当し、医薬品医療機器等法により規制されます。日赤では医薬品医療機器等法に基づき、輸血による副作用や感染症等の情報を収集し、これらの評価検討を実施し、重篤な副作用等症例については厚生労働大臣に報告している他、製剤の回収、添付文書(使用上の注意)改訂、MRを通じた医薬関係者への情報提供等の一連の業務を行っています。また、採血副作用についても事例の収集・検討を行っています。これらと並行して、血液の安全性に関連する疫学調査を行い、その結果については国の薬事・食品衛生審議会血液事業部会の運営委員会や安全技術調査会等へ報告し、輸血用血液の安全対策に視するよう努めています。以上のような活動を包括したものが日本のヘモビジランスシステムとなります。
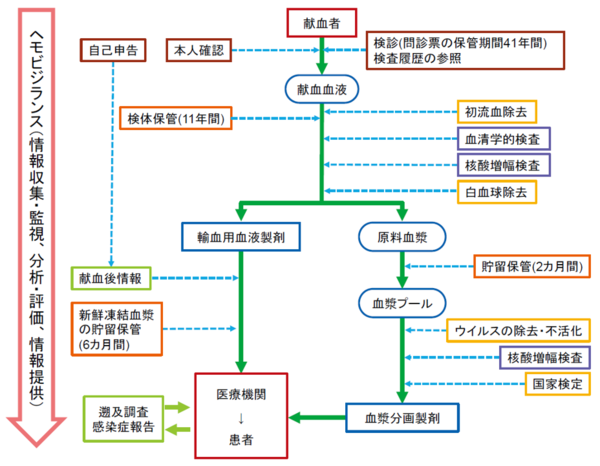
日赤では1993年に輸血副作用・感染症情報を一元的に収集し解析する体制を構築し、ヘモビジランス活動を行ってきました。現在は、血液事業本部、各血液センター、中央血液研究所の各施設が分担協力し、情報の収集・分析・評価を行っています。医療機関からの副作用等情報収集や医薬関係者への輸血用血液製剤に関する情報提供には各血液センターの医薬情報担当者(MR)が当たっています。日赤の調査体制の最大の特徴は、すべての献血血液についてその一部を調査用の検体として11年間保管していることであり、1996年9月から実施しています。この検体保管は、副作用および感染症にかかる輸血用血液製剤の調査を可能とし、その因果関係を確認する手段であるとともに、将来、新たに発生するかもしれない感染症や副作用に対しての調査においても有用です。また、献血者、採血、検査、製造および供給に関するデータについては、コンピューターシステムにより全国的に一元管理しており、データベースは献血時の履歴参照および遡及調査等に活用しています。
また、採血時の副作用については、日赤が血液事業を開始した昭和20年代から予防対策を講じ、採血を担当する看護師を対象とした研修等を実施してきました。採血副作用の報告は1982年には社内手順として規定され、現在はコンピューターシステムにより全国的に一元管理を行っています。
採血(献血者)から輸血(患者)への流れと安全対策
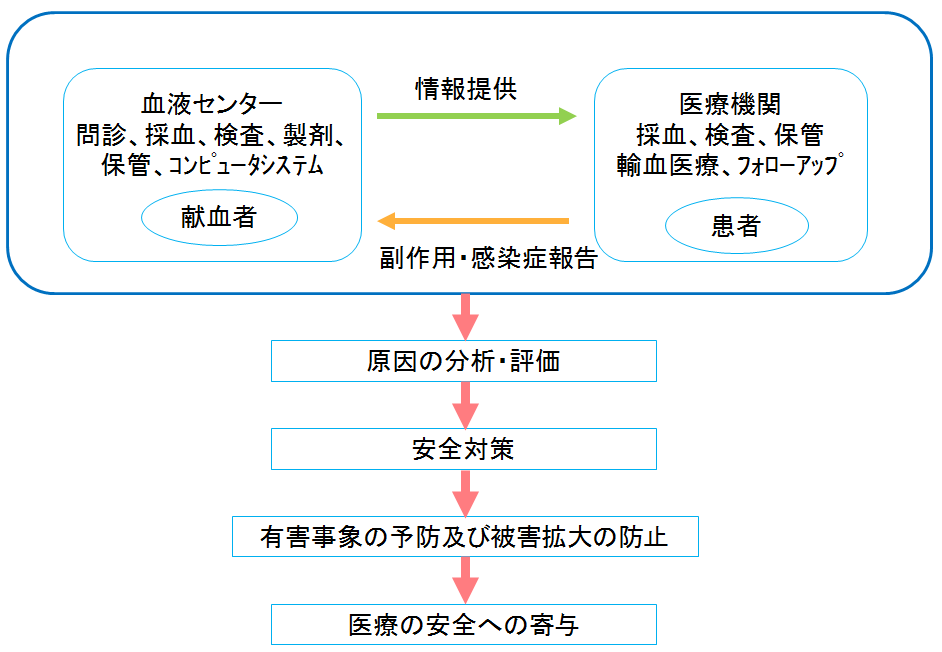
情報提供と安全性の向上
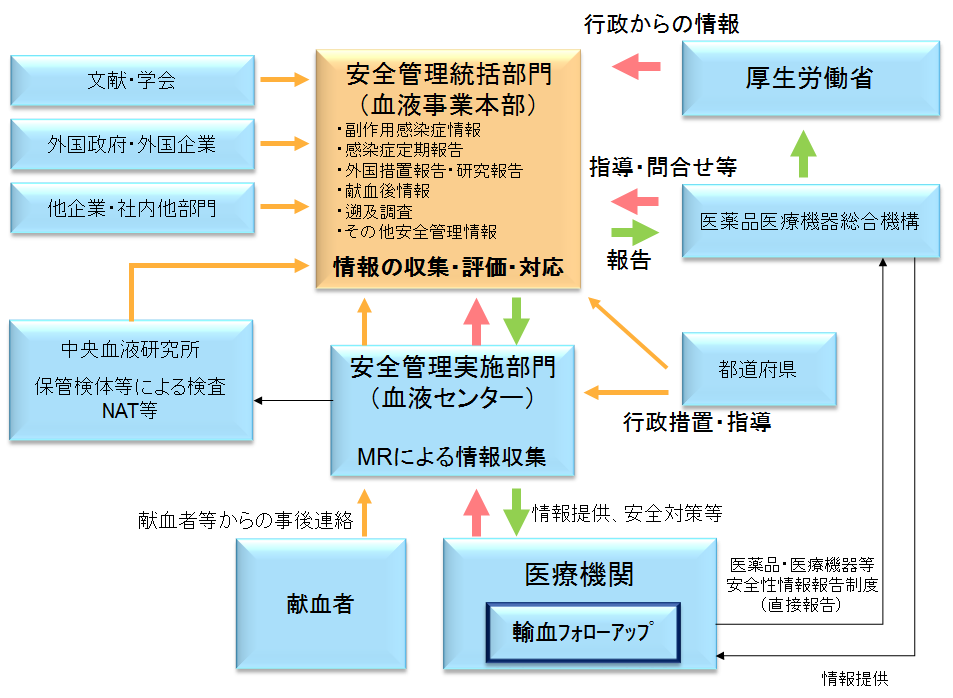
情報収集と報告(提出)の流れ
参考リンク
ISBT Haemovigilance working party